සමස්ථානික
එකම මූලද්රව්යයක වෙනස් නියුට්රෝන සංඛ්යාවන් සහිත වෙනස් පරමාණුක න්යෂ්ටීන් පවතී නම් ඒවා සමස්ථානික ලෙස හැඳින්වේ. එනම් සමස්ථානික වල සමාන ප්රෝටෝන සංඛ්යාවක් තිබුණ ද වෙනස් නියුට්රෝන සංඛ්යාවන් ඇත. ස්වභාවිකව පවතින බොහෝ මූලද්රව්ය සඳහා (94 න් 66 ක්ම) එක් ස්ථායී සමස්ථානිකයකට වඩා වැඩි ප්රමාණයක් ඇත. උදාහරණයක් ලෙස කාබන්වලට නියුට්රෝන 6ක්, 7ක්, හා 8ක් ඇති ප්රධාන සමස්ථානික තුනක් ඇත.
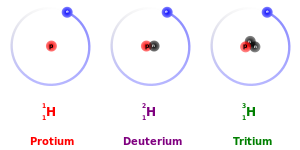

සමස්ථානික හඳුන්වන්නේ මූලද්රව්යයේ නම අගට කෙටි ඉරක් සහ සමස්ථානිකයේ ස්කන්ධ ක්රමාංකය ලිවීමෙනි (උදා: හීලියම්-3, හීලියම්-4, කාබන්-12, කාබන්-14, යුරේනියම්-235 සහ යුරේනියම්-239).
මූලද්රව්යයක ස්වභාවයෙන් ස්ථායී වන සමස්ථානික ස්ථායී සමස්ථානික ලෙස ද, ස්ථායි නොවන සමස්ථානික විකිරණශීලී සමස්ථානික ලෙස ද හැඳින්වේ. සමහර සමස්ථානික විකිරණශීලී වන අතර ඇල්ෆා අංශු හෝ බීටා අංශු විමෝචනය කිරීම මගින් වෙනත් මූලද්රව්යයන්ට තත්වාන්තරණය වේ. උදාහරණයක් ලෙස කාබන්-14 විකිරණශීලී වේ. සමහර මූලද්රව්යවල සියලුම සමස්ථානික විකිරණශීලී සමස්ථානිකයි. ටෙක්නීෂියම් (පරමාණුක ක්රමාංකය 43), ප්රොමේතියම් (පරමාණුක ක්රමාංකය 61) සහ පරමාණුක ක්රමාංකය 82 ට වැඩි නිරීක්ෂිත සියලුම මූලද්රව්යය වල සියලුම සමස්ථානික විකිරණශීලී වේ.
ස්ථිර සමස්ථානික සහිත මූලද්රව්ය 80 න් 16 කම ඇත්තේ එක් ස්ථායී සමස්ථානියක් පමණි. ස්ථායී මූලද්රව්ය 80 සඳහා ස්ථායී සමස්ථානිකවල මධ්යනය අගය එක් මූලද්රව්යයකට ස්ථායී සමස්ථානික 3.4ක් වේ. මූල ද්රව්යයකට ඇති ස්ථායී සමස්ථානික උපරිම සංඛාවක් ඇති ටින් (පරමාණුක ක්රමාංකය 50) මූලද්රව්යයට ස්ථායී සමස්ථානික 10ක් ඇත.
අමතර අවධානයට
සංස්කරණයමූලාශ්ර
සංස්කරණයභාහිර සබැඳි
සංස්කරණය- The Nuclear Science web portal Nucleonica
- The Karlsruhe Nuclide Chart
- National Nuclear Data Center Portal to large repository of free data and analysis programs from NNDC
- National Isotope Development Center Coordination and management of the production, availability, and distribution of isotopes, and reference information for the isotope community
- Isotope Development & Production for Research and Applications (IDPRA) U.S. Department of Energy program for isotope production and production research and development
- International Atomic Energy Agency Homepage of International Atomic Energy Agency (IAEA), an Agency of the United Nations (UN)
- Atomic Weights and Isotopic Compositions for All Elements Static table, from NIST (National Institute of Standards and Technology)
- Atomgewichte, Zerfallsenergien und Halbwertszeiten aller Isotope
- Exploring the Table of the Isotopes at the LBNL
- Current isotope research and information isotope.info
- Emergency Preparedness and Response: Radioactive Isotopes by the CDC (Centers for Disease Control and Prevention)
- Chart of Nuclides සංරක්ෂණය කළ පිටපත 2018-10-10 at the Wayback Machine Interactive Chart of Nuclides (National Nuclear Data Center)
- Interactive Chart of the nuclides, isotopes and Periodic Table සංරක්ෂණය කළ පිටපත 2008-09-30 at the Wayback Machine
- The LIVEChart of Nuclides – IAEA with isotope data.
- Annotated bibliography for isotopes from the Alsos Digital Library for Nuclear Issues
- The Valley of Stability (video) – a virtual "flight" through 3D representation of the nuclide chart, by CEA (France)