අයන
අයනයක් (ඉංග්රීසි: ion) යනු, පරමාණුවක මුළු ඉලෙක්ට්රෝන ගණන එහි මුළු ප්රෝටෝන ගණනට සමාන නොවීම නිසා, එයට දළ ධන හෝ සෘණ හෝ විද්යුත්මය ආරෝපණයක් ලබා දී ඇති පරමාණුවක් හෝ අණුවකි.
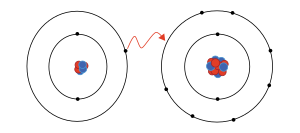
භෞතික හෝ රසායනික හෝ ක්රම වලින් අයන තැනිය හැකි වෙයි. රසායනික භාවිතයෙහිදී, උදාසීන පරමාණුවක් විසින්, එකක් හෝ වැඩි ගණනක් ඉලෙක්ට්රෝන අහිමි කර ගනී නම්, එය වෙත දළ ධන ආරෝපණයක් හිමි වන අතර එවැන්නක් කැටායනයක් ලෙසින් හැඳින්වෙයි. පරමාණුවක් විසින් ඉලෙක්ට්රෝන ග්රහණය කර ගනී නම්, එය වෙත දළ සෘණ ආරෝපණයක් හිමි වන අතර එවැන්නක් ඇනායනයක් ලෙසින් හැඳින්වෙයි. තනි පරමාණුවක් සහිත අයනයක් පරමාණුක හෝ ඒකපරමාණුක අයනයක් වෙයි; එය පරමාණු දෙකකින් හෝ වැඩි ගණනකින් සමන්විත වෙයි නම්, එය අණුක හෝ බහුපරමාණුක අයනයක් වෙයි.
වායුවක් වැනි මාධ්යයක් භෞතික වශයෙන් අයනීකරණය කිරීමේදී, අයන ගැටීම නිසාවෙන් "අයන යුගල" ලෙසින් හඳුන්වන්න තැනෙන අතර එක් එක් යුගලය සමන්විත වන්නේ නිදහස් ඉලෙක්ට්රෝනයක් සහ ධන අයනයකිනි.[1]
අනායන සහ කැටායන
සංස්කරණයප්රෝටෝනයක් වෙත ඇති විද්යුත් ආරා්පණය විශාලත්වය අතින් ඉලෙක්ට්රෝනයක ආරෝපණයට සමාන බැවින්, අයනයක් වෙක ඇති දළ විද්යුත් ආරෝපණය, එහි ඇති ප්රෝටෝන ගණන සෘණ ඉලෙක්ට්රෝන ගණනට සමාන වෙයි.
"ඉහළ" යන අදහස දෙන, ἄνω (ඇනෝ) යන ග්රීක වචනයෙන් බිඳී එන, ඇනායනයක් (−) යනු, ප්රෝටෝන වලට වඩා ඉහළ සංඛ්යාවක් ඉලෙක්ට්රෝන තිබීම නිසා, දළ සෘණ ආරෝපණයක් (ඉලෙක්ට්රෝන සෘණ ආරෝපිත සහ ප්රෝටෝන ධන ආරෝපිත නිසා) සහිත අයනයකි.
"පහළ" යන අදහස දෙන, κατά (කැටා) යන ග්රීක වචනයෙන් බිඳී එන, කැටායනයක් (+) යනු , ප්රෝටෝන වලට වඩා පහළ සංඛ්යාවක් ඉලෙක්ට්රෝන තිබීම නිසා, දළ ධන ආරෝපණයක් පවතින අයනයකි.
බහු ගුණ සංඛ්යාවක් ආරෝපණ පවතින අයන සඳහා අමතර නම් පවතියි. නිදසුනක් ලෙසින්, −2 ආරෝපණයක් පවතින අයනයක් හැඳින්වෙන්නේ ද්වීඇනායනයක් ලෙසින් වන අතර +2 ආරෝපණයක් පවතින අයනයක් ද්වීකැටායනයක් ලෙසින් හැඳින්වේ. ද්වීකායනයක් යනු අණුව තුල වෙනස් තන්හී ධන සහ සෘණ ආරෝපණ පවතින උදාසීන අණුවකි.
සොයාගැනීමේ ඉතිහාසය
සංස්කරණයඅයනය යන්නට ඉංග්රීසි පදය වන අයන් යන වචනය, ιεναι, ienai, "යෑමට" යන්නෙහි මිශ්ර ක්රියාව වන ග්රීක ιον (යාම) යන්නෙන් බිඳී එයි. එක් ඉලෙක්ට්රෝඩයක් වෙතින් අනෙකකට ජලීය මාධ්යයක් තුලින් යන එකල-නොහඳුනන විශේෂිතය සඳහා 1834දී ඉංග්රීසි භෞතික විද්යාඥ සහ රසායන විද්යාඥ මයිකල් ෆැරඩේ විසින් මෙම පදය හඳුන්වාදෙන ලදි. [2][3] මෙම විශේෂිතයන්ගේ ස්වභාවය ෆැරඩේ විසින් නොදැන සිටි නමුදු, එක් ඉලෙක්ට්රෝඩයක් වෙතෙහි ලෝහ දියවී ද්රාවණයට එක් වන බවද, ද්රාවණය වෙතින් නව ලෝහයක් අනෙක් ඉලෙක්ට්රෝඩය වෙතෙහිදී පැමිණෙන බවද දැන සිටි හෙතෙම, එක් තැනක සිට තවත් තැනකට පදාර්ථය ගෙන යමින්, කිසියම් ආකාරයක ද්රව්යයක් ධාරාවක ස්වභාවයෙන් ද්රාවණය තුලින් ගමන් කරන බැව් දැන සිටියේය.
සෘණ ආරෝපිත අයනයකට ඇනායනය යන වචනයද, ධන ආරෝපිත අයනයකට කැටායනය යන වචනයද ෆැරඩේ විසින් හඳුන්වා දුනි. ෆැරඩේගේ නාමකරණයට අනුව, ගැල්වානික උපකරණයක කැතෝඩය වෙත ආකර්ෂණය වන නිසා කැටායන වලට එම නමද ආනෝඩය වෙත ආකර්ෂණය නිසා ඇනායන වලට එම නමද ලැබුණි.
ගුණාංග
සංස්කරණයඔවුන්ගේ වායු-වැනි තත්ත්වයෙහිදී අයන අතිශයින් සක්රීය වන අතර, ගිනි දැල්, අකුණු, විදුලි පුළිඟු, සහ අනෙකුත් ප්ලාස්මාවන්හිදී හැර, පෘථිවිය මත විශාල ප්රමාණ වලින් ඇති නොවෙයි. මෙම වායු-වැනි අයන විගසින් ප්රතිවිරුද්ධ ආරෝපණ අයන හා ප්රතික්රියා කරන්නේ උදාසීන අණු හෝ අයනික ලවණ තැනීමටය. ලවණ වර්ග ද්රාවක (නිදසුනක් වශයෙන්, ජලය) සමග අන්තර්ක්රියා කරමින් "ද්රාවක අයන" සදන විටදී, ද්රව සහ ඝණ අවස්ථාවෙහි පවතින අයන තැනෙන අතර, ද්රවය සමග අන්තර්ක්රියා සිදුකිරීම සඳහා එකිනෙක වෙතින් අයන ඈත් වීම හා සම්බන්ධ ශක්ති හා එන්ට්රොපි වෙනස්කම් වල සංකලනයක් වන හේතු කරුණු නිසා ඒවා වඩාත් ස්ථායි වෙති. මෙම ස්ථායී විශේෂිතයන් සාමාන්ය වශයෙන් අඩු උෂ්ණත්ව පරිසරයන්හී දක්නට ලැබේ. සුලබ නිදසුනක් වන්නේ, මුහුදු ජලයේ දක්නට ඇති, ද්රාව්ය අයන වලින් ව්යුත්පන්නව ඇති, අයන වෙයි.
සියළු අයන ආරෝපිත වන අතර, එයින් ගම්ය වන්නේ ආරෝපිත සියළු වස්තූන් මෙන්ම, ඒවාද:
- විරුද්ධ ආරෝපණ වලට (සෘණ වෙත ධන, සහ සහ ප්රතිලෝම වශයෙන්) ආකර්ෂණය වෙති,
- සමාන ආරෝපණ වලින් විකර්ෂණය වෙති
- චලනය වන විට, චුම්බක ක්ෂේත්රයකින් උත්ක්රමය කල හැකි පථයන්හී ගමන් කරති.
එහි කුඩා ප්රමාණය සහ පදාර්ථ තරංග ලෙසින් එහි අවකාශ-පිරවීමේ මහත් ගුණාංගය නිසා, කුමන හෝ ප්රමාණයක ඉලෙක්ට්රෝන අඩංගු පරමාණු සහ අණුවල විශාලත්වය තීරණය කිරීම ඉලෙක්ට්රෝන විසින් සිදු කෙරෙයි. එමනිසා, ඇනායන (සෘණ ආරෝපිත අයන) එහි පිතෘක අණුව හෝ පරමාණුවට වඩා විශාල වන්නේ, අතිරික්ත ඉලෙක්ට්රෝන (ය) එකිනෙක විකර්ෂණය කරන නිසා සහ, එහි ඉලෙක්ට්රෝන වලාවේ ප්රමාණය විසින් එහි විශාලක්වය තීරණය කරන නිසා, අයනයේ භෞතික විශාලත්වය අධික වීම සිදු වන බැවිනි. මෙම හේතුව නිසා පොදු ලෙසින්, අදාල පිතෘක පරමාණු හෝ අණුවලට වඩා කැටායන කුඩා වන්නේ ඉලෙක්ට්රෝන වලාවේ කුඩා විශාලත්වය නිසාය. එක් සුවිශේෂී කැටායනයක් (හයිඩ්රජන් හී) ඉලෙක්ට්රෝන රහිත වන අතර, එම නිසා පිතෘක හයිඩ්රජන් පරමාණුවට වඩා බෙහෙවින් කුඩා වෙයි.
ස්වභාවික පැවතීම්
සංස්කරණයස්වභාවධර්මයේ සාර්වචක්රවර්තික වන අයන, සූර්යයාගේ සංදීප්තියෙහි සිට පෘථිවියෙහි අයනගෝලය පැවැත්ම දක්වා විවිධවූ සංසිද්ධීන් ගණනාවකට වගකියයි. අයනික අවස්ථාවෙහි පවතින පරමාණු, උදාසීන පරමාණු වලට වඩා වෙනස් පැහැයක් ගත හැකි අතර, එබැවින්, ලෝහ අයන වලින් ආලෝකය අවශෝෂණය කිරීම නිසා මැණික් වලට වර්ණය ලබා දෙයි.
මේවාත් බලන්න
සංස්කරණයආශ්රිත
සංස්කරණය- ^ Knoll, Glenn F (1999). Radiation detection and measurement (3rd ed.). New York: Wiley. ISBN 0-471-07338-5.
- ^ මයිකල් ෆැරඩේ (1791-1867). එරා: බීබීසී. http://www.bbc.co.uk/history/historic_figures/faraday_michael.shtml.
- ^ "ඔන්ලයින් එටිමොලජි ඩික්ෂනරි". සම්ප්රවේශය 2011-01-07.